|
CONTRACCIONES VENTRICULARES PREMATURAS : ¿SON TODAS
IGUALES? |
|
Santiago
García-Velasco Sánchez-Morago |
|
Servicio
de Medicina Intensiva. Hospital General de Ciudad
Real |
Las contracciones ventriculares prematuras son latidos precoces
que se producen por un foco ectópico situado en los ventrículos
y que se adelantan al ritmo de base del paciente. Al encontrarse
su origen en el ventrículo la activación no se produce por las
vías específicas de conducción, produciéndose un complejo QRS
ancho al incrementarse el tiempo necesario para activar ambas
cavidades ventriculares. Existen numerosas clasificaciones de
esta arritmia que puede ser fácilmente identificada ya sea en la
monitorización del paciente o en la realización de un
electrocardiograma de doce derivaciones.
PALABRAS
CLAVE: Contracciones ventriculares prematuras,
enfermería, electrocardiografía, extrasístoles
ventriculares.
Definimos extrasístole como todo latido precoz que se adelanta
al latido que presuntamente debería aparecer en el registro del
electrocardiograma (ECG) por el ritmo de base del paciente (1).
Si el latido nace en un foco ectópico del ventrículo lo
denominamos contracción ventricular prematura (CVP) o
extrasístole ventricular (EV) (2).
Las CVP constituye n las arritmias más frecuentes,
pudiendo observarse en el ECG en un 5% y en el Holter de
24 horas en un 50% de los pacientes sanos. Si existe
cardiopatía previa estas cifras aumentan a un 10% en el
ECG y a un 60-90% en el Holter. Las características
morfológicas de la CVP, su asociación entre sí y con el
ritmo base, permiten realizar una clasificación de las
mismas y estimar el grado de peligrosidad que presentan
(3). El paciente puede notar estos latidos como un
vuelco de corazón, una sensación de vacío o un golpeteo
en el pecho, aunque muchas veces su hallazgo es casual y
no tiene importancia (4).
Las causas que generan las CVP son variadas, pudiendo observarse
en sujetos sanos, además de pacientes cardiópatas con
cardiopatía isquémica e hipertensiva, en el contexto del
síndrome coronario agudo, miocardiopatías, pericarditis e
insuficiencia cardiaca. En causas extracardíacas podemos
destacar la hipoxia, edema de pulmón, enfermedad pulmonar
crónica, estados acidóticos, trastornos electrolíticos (hipomagnesemia
e hipocalemia), la estimulación adrenérgica (incluido el uso de
fármacos vasoactivos), antiarrítmicos (digital, quinidina,
procainamida) y otros fármacos (fenotiazidas y antidepresivos
tricíclicos) (5).
Las características definitorias de las CVP incluyen,
además de su origen en el territorio ventricular :
1.
Prematuridad: Dentro de la precocidad de las CVP, pueden
clasificarse como:
a.
Protodiastólicos : son latidos muy precoces en los que
la CVP coincide con la rama descendente de la onda T del
latido precedente. Este fenómeno se conoce como fenómeno
R sobre T (6). Son considerados muy peligrosos puesto
que la rama descendente de la onda T es periodo
refractario relativo del ciclo cardiaco, y cualquier
estímulo que incida sobre ella puede desencadenar una
respuesta repetitiva como taquicardias ventriculares o
lo que es aún más peligroso fibrilación ventricular (FV).
b.
Mesodiastólicos : son moderadamente precoces dentro de
la prematuridad.
c.
Telediastólicos : son latidos poco precoces (definidos
como “tardíos” dentro de la precocidad) adelantándose
por muy poco al complejo QRS del latido siguiente, pero
no logra adelantarse a la onda P de dicho latido,
cayendo sobre el intervalo PR, denominándose CVP del PR.
2.
Configuración deformada del QRS: es un complejo ancho
(>0.12 seg.), aberrado, al no seguir las vías de
conducción específicas del corazón. Según el lugar donde
se encuentre el foco ectópico nos encontraremos (7):
a. Si el
foco de la CVP se encuentra en el ventrículo derecho la
morfología será de bloqueo de rama izquierda (BRI)
debido a que la activación será similar a esta
patología.
b. De la
misma forma si la CVP se origina en el ventrículo
izquierdo (VI) tendrá morfología de bloqueo de rama
derecha (BRD).
c. Puede
ser que la CVP se produzca cerca de las ramas del Haz de
His (CVP fasciculares) siendo la morfología del QRS
estrecha y variable.
d. Cuando
el foco se encuentra en la pared posterior del VI la CVP
tiene morfología de BRD con hemibloqueo anterior
izquierdo (HAI).
e. Si el
origen es la cara anterior la morfología es de BRD más
hemibloqueo posterior izquierdo (HPI).
f. Si se
producen en el ápex, la CVP tendrá complejos negativos
en todas las derivaciones precordiales, y en los
miembros el eje del QRS esta desviado a la derecha si se
origina en la cara posterior del ápex y hacia abajo si
se origina en la cara anterior del ápex.
3.
Cambios secundarios del segmento ST y onda T: la onda de
repolarización mantiene una polaridad opuesta al
complejo QRS.
4. Los
efectos sobre el ritmo de base del paciente pueden ser
(8):
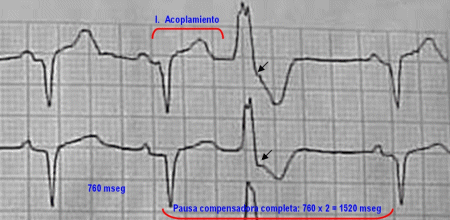
a. Pausa
compensadora completa: la distancia que existe entre el
latido precedente y posterior a la CVP es el doble de un
ciclo base del ritmo del paciente.
b.
Interpolación: la CVP se sitúa entre dos latidos del
ritmo del paciente y el intervalo de acoplamiento y la
pausa compensadora miden lo mismo, lo que hace que el
registro sea rítmico.
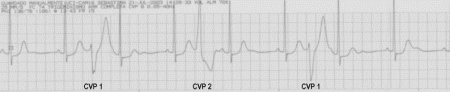
5.
Tendencia a intervalo acoplamiento fijo: el intervalo de
acoplamiento se define como la distancia que existe
entre el inicio del complejo QRS del latido precedente y
el inicio del complejo QRS de la CVP. Este intervalo es
constante para cada CVP (con una variación no superior a
0.08 seg. para un mismo foco), con lo cual se pueden
definir CVP:
a.
Unifocales: el intervalo de acoplamiento es constante en
todas las CVP debido a que su origen es un único foco.
La morfología de la CVP es idéntica en todo el trazado.
b.
Multifocales: cada foco ectópico tiene un intervalo de
acoplamiento diferente, siendo la morfología de las CVP
diferentes en la misma derivación.
c.
Parasistolia: existen dos o más focos independientes en
los ventrículos con periodos de acoplamiento diferentes,
que no se ven afectados entre sí, observándose en el ECG
la resultante de la actividad de todos ellos.
6.
Activación auricular retrógrada: en algunas ocasiones
puede producirse una activación retrógrada de las
aurículas que se registra en el ECG como una onda P que
no se visualiza o en ocasiones se encuentra inscrita
dentro del QRS de la CVP (9).
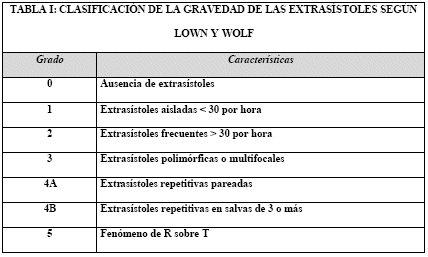
En 1971 Lown y Wolf propusieron una clasificación de
acuerdo con el grado de gravedad de la extrasistolia
ventricular (10), siendo el estadio menos grave la
aparición de CVP aisladas y la más grave las CVP con
fenómeno de R sobre T. Aunque esta clasificación ha sido
muy discutida por numerosos autores, hoy en día sigue
siendo clínicamente válida.
1.
Extrasístoles frecuentes: se denominan así cuando
aparecen en los registros con una frecuencia de más de
30 CVP por hora (o más de 5 CVP por minuto).
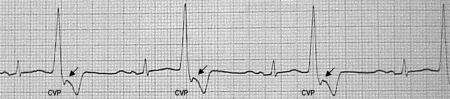
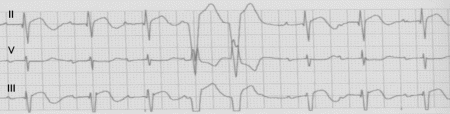
2.
Bigeminismo ventricular: Consiste en la alternancia de
un latido sinusal con uno extrasistólico con un
acoplamiento constante entre los pares de latidos
sinusales y las CVP (Imagen 3). A veces estas CVP se ven
favorecidas si el intervalo RR precedente es largo.
Además al dejar la extrasístole la pausa compensadora,
aparece un nuevo intervalo RR alargado que permite
perpetuar el bigeminismo. Este fenómeno en el que el
ritmo bigeminado depende del intervalo RR precedente a
la extrasístole se conoce como regla del bigeminismo.
3.
Trigeminismo ventricular: la alternancia se produce con
dos latidos sinusales y uno extrasistólico, con la misma
condición que el bigeminismo.
4. Pareja
de CVP o dobletes: Es la sucesión de dos extrasístoles
consecutivas.
5.
Triplete de CVP: Consiste en la aparición de tres CVP
consecutivas. Si en algún registro aparecen más de tres
CVP consecutivas con la misma morfología y una
frecuencia superior a los 100 latidos/minuto
(generalmente entre 150-250) nos encontraríamos con una
salva de taquicardia ventricular extrasistólica (11,12).
Ante problemas diagnósticos, debe realizarse el
diagnóstico diferencial con las siguientes patologías :
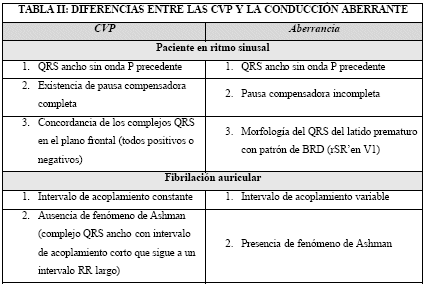
-
Conducción ventricular aberrante en el seno de un
ritmo sinusal: se producen latidos precoces con
pausa compensadora incompleta, suele poder
observarse la onda P que precede al complejo QRS y
como la aberrancia (que es la conducción anormal de
un impulso supraventricular a los ventrículos) suele
producirse en la rama derecha del Haz de His, la
morfología del latido prematuro será de BRD (en V1
morfología rSR’). La concordancia de polaridad de la
CVP en las derivaciones precordiales (todas
positivas o todas negativas) apunta la posibilidad
hacia el diagnóstico de extrasistolia ventricular.
-
Conducción ventric ular aberrante en el seno de una
fibrilación auricular: su diagnóstico se basa en
intervalos de acoplamiento variable, no dejan pausa
compensadora completa y la morfología del QRS en V1
es rSR’.
Generalmente, y siempre contando con que no exis ta
patología estructural, no precisan de tratamiento. Si el
paciente presente conjuntamente otras arritmias
ventriculares y se encuentra estable hemodinámicamente,
el tratamiento médico se realiza con antiarrítmicos
como:
Lidocaína:
Antiarrítmico clase Ib (estabilizador de membrana -bloqueante
de los canales del calcio- con potencia ligera en el
enlentecimiento de la conducción), utilizado
principalmente para tratar las arritmias ventriculares
(siendo muy eficaz en la supresión de las arritmias por
reentrada como los extrasístoles ventriculares y la
taquicardia ventricular), con efectos mínimos en las
arritmias supraventriculares. Su principal vía
metabólica es el hígado y la eliminación es renal.
Amiodarona: Antiarrítmico clase III, que alarga la
duración del potencial de acción bloqueando los canales
de potasio. Enlentece el automatismo sinusal, disminuye
la excitabilidad cardiaca, prolonga el periodo
refractario y disminuye la conducción AV. Además produce
vasodilatación arterial periférica, con hipotensió n y
disminución de la postcarga. Se emplea en el tratamiento
de arritmias supraventriculares y ventriculares. Puede
provocar diferentes grados de BAV y alargamiento del
intervalo QT.
Procainamida: Antiarrítmico clase Ia que actúa
bloqueando los canales de sodio, sus efectos son el
alargamiento del periodo refractario y de la duración
del potencial de acción de la aurícula, His y
ventrículo. Disminuye el automatismo, la excitabilidad
la velocidad de conducción y contracción miocárdicos,
con efectos anticolinérgicos. Puede producir un síndrome
de pseudolupus (síndrome eritematoso lupus- like), que
desaparece al suspender el tratamiento.
Con un poco de entrenamiento y práctica diaria es
posible reconocer la actividad ectópica ventricular,
mejorando así en nuestra actividad cotidiana, prestando
una mejor atención integral a nuestros pacientes.
1. Olgin
J, Zipes D. Arritmias específicas: diagnóstico y
tratamiento. En: Braunwald E, Zipes D, Lobby P,
editores. Braunwald’s Cardiología. Madrid: Marbán,
2004:1043-6.
2. Karnes,
Nancy J. Contracciones ventriculares prematuras: cuando
suena la alarma. Nursing. 1985 abr. 3(3):9-13.
3.
Docherty B, Douglas M. Cardiac care: 3. ECG
interpretation - ventricular arrhythmias. Prof Nurse.
2003 Apr;18(8):459-61.
4. Moreno
Gómez R, García Fernández A: Electrocardiografía.
Madrid: McGraw-Hill, 1999:55.
5.
Castellano C, Pérez de Juan MA, Espinosa JS:
Electrocardiografía Clínica. Madrid: Mosby- Doyma,
1996:276-86.
6.
Rodríguez Padial L: Curso básico de Electrocardiografía.
Madrid: Jarpyo Ed, 1999:183-93.
7. García
Niebla J. Electrocardiografía extrasistólica. Rev Enferm
Cardiol. 2003 ene-abr. 28:25-8.
8. Sims
JM, Miracle V. Premature ventricular contractions.
Nursing. 1997 Aug;27(8):43.
9. Moro
C, Hernández Madrid A, García Cosio F.
Electrocardiografía clínica. Madrid: McGraw-Hill, 2001.
8:161-169.
10. Lown
B, Wolf M. Approaches to sudden death from coronary
heart disease. Circulation. 1971 Jul;44(1):130-42.
11.
Camphell CD, Newsome JA. Detección de arritmias
potencialmente letales. Nursing. 1991 nov. 9(9):24-30.
12.
Albert NM. Ventricular dysrhythmias in heart failure. J
Cardiovasc Nurs. 2004 Nov- Dec;19(6 Suppl):S11-26.
|